Par le Dr Mina Petkova
Patient de 68 ans, adressé pour déficit sensitif transitoire brachiofacial gauche et troubles mnésiques.
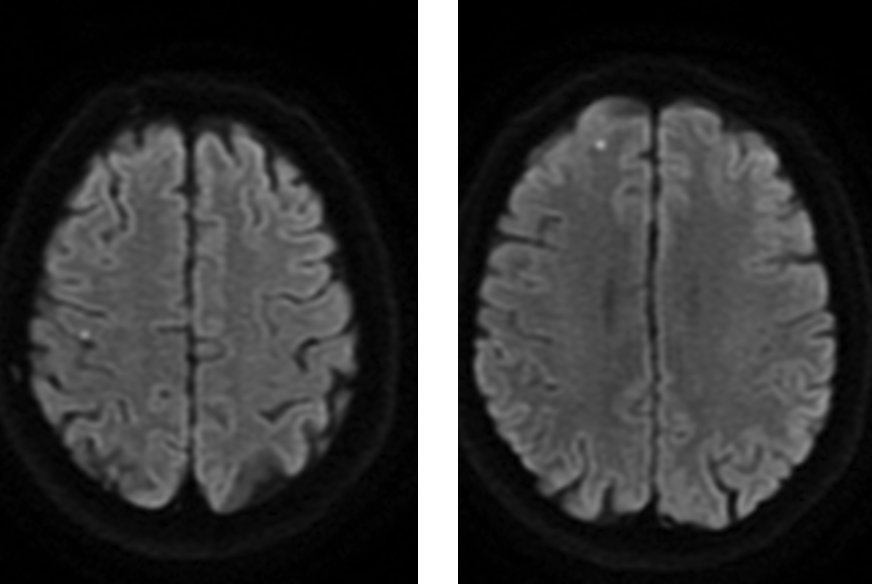
L’IRM montre deux hypersignaux diffusion punctiformes frontaux droits témoignant de micro infarctus cérébraux aigus, un hypersignal FLAIR dans les espaces sous-arachnoïdiens fronto-pariétaux droits en rapport avec une hémorragie sous-arachnoïdienne aiguëmais également des saignements anciens en hyposignal T2* dans les espaces sous-archnoïdiens fronto-pariétaux, des microsaignements anciens cortico-sous-corticaux et une minime leucopathie périventriculaire.
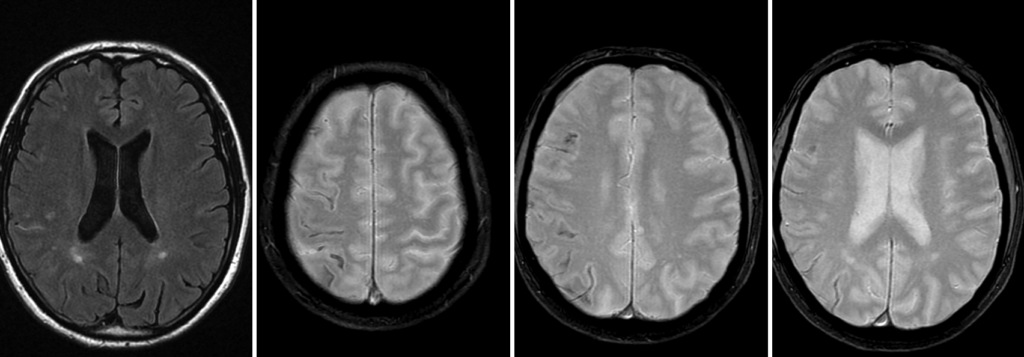
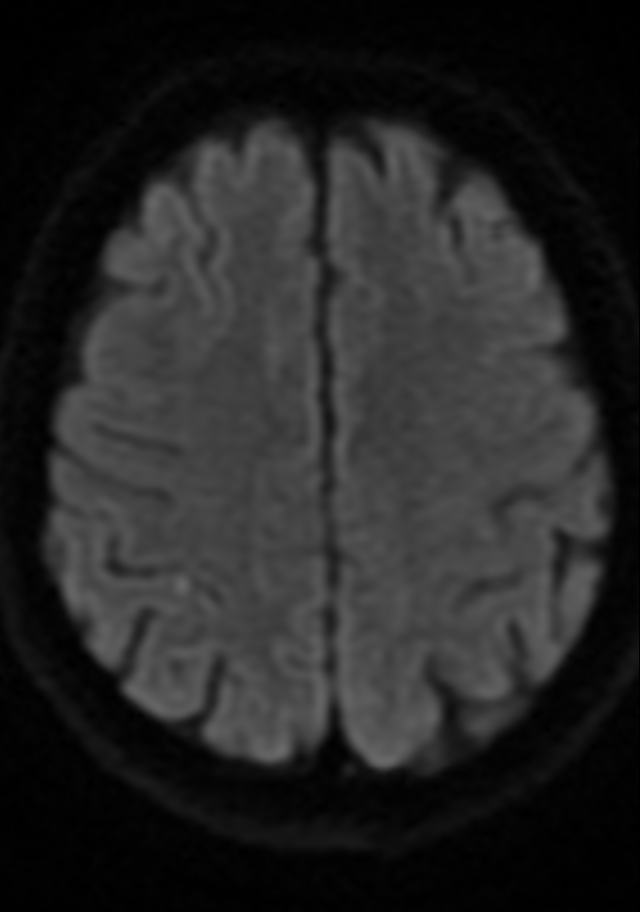
Sur l’IRM réalisée 3 ans plus tard on observe une nette majoration des stigmates hémorragiques anciens dans les espaces sous-arachnoïdiens et des hémorragies lobaires.
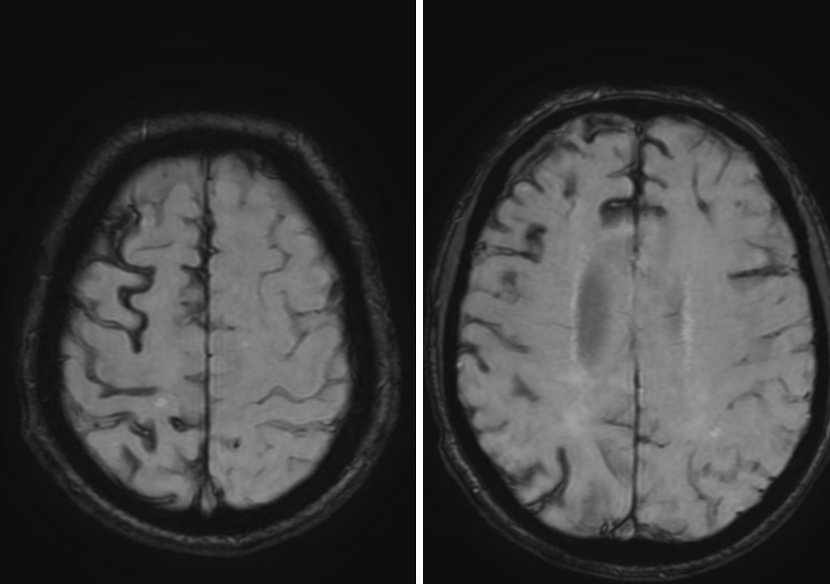
L’angiopathie amyloïde cérébrale (AAC) est une maladie du sujet âgé qui se caractérise par des dépôts de protéine ß-amyloïde dans la paroi des vaisseaux corticaux et leptoméningés de petit et moyen calibre. L’AAC est une maladie hémorragique et ischémique. Elle est la 2e cause d’hémorragie cérébrale chez les patients de plus de 60 ans particulièrement chez les sujets normotendus mais également une cause majeure de déclin cognitif chez le sujet âgé. Malgré sa haute prévalence, l’AAC reste une cause sous-estimée de maladies cérébro-vasculaires.
Les dépôts amyloïdes sont liés à une surproduction ou un défaut de dégradation du peptide Aβ, un produit de la protéolyse d’un récepteur membranaire codée par le chromosome 21. Des dépôts amyloïdes se forment d’une part entre les neurones entraînant la formation de plaques séniles, d’autre part dans la paroi vasculaire, ce qui explique la coexistence fréquente de l’AAC avec la tauopathie mais le continuum entre les deux n’est pas clairement établi. Les dépôts dans la paroi vasculaire sont responsables d’une perte des cellules musculaires lisses, d’un épaississement de la paroi, d’un rétrécissement de la lumière vasculaire, d’une dissociation concentrique de la paroi, de la formation de micro-anévrysmes et de microhémorragies péri-vasculaires.
L’AAC est le plus souvent asymptomatique et peut être révélée par des microsaignements (microbleeds) à l’IRM.
Elle peut se manifester par des hémorragies lobaires souvent récidivantes, révélées par des céphalées, déficit focaux, crises convulsives, troubles de la conscience. Leur topographie est le plus souvent frontale. L’AAC est la cause la plus fréquente d’hémorragie lobaire chez le sujet âgé.
L’AAC peut également être responsable d’hémorragie sous-arachnoïdienne non-traumatique, de petits infarctus cérébraux révélés par des déficits neurologiques transitoires ou de troubles cognitifs.
L’IRM est l’examen le plus pertinent pour le diagnostic avec la séquence T2* sensible aux produits de dégradation de l’hémoglobine qui peut montrer des hématomes lobaires, des microsaignements en hyposignal T2* de distribution périphérique, cortico-sous-corticaux et sous-arachnoïdiens (ce qui distingue l’AAC de la microangiopathie hypertensive), une leucopathie et des micro infarctus aigus.
Selon les critères diagnostiques de Boston l’AAC est probable chez un patient ≥ 55 ans, ayant deux hémorragies cérébrales lobaires corticales ou sous-corticales (ou une hémosidérose corticale) sans autre cause d’hémorragie et possible dans les mêmes conditions en cas d’hémorragie cérébrale unique lobaire corticale ou sous-corticale (ou une hémosidérose corticale).
Il est conseillé d’arrêter ou d’éviter les traitements antithrombotiques, antiagrégants plaquettaires et anticoagulants et de maîtriser la tension artérielle.
Références :
- Alamowitch S. Sang Thrombose Vaisseaux 2007
- Alafuzoff I. Stroke 2008
- Chao CP. Radiographics 2006
- CEN 2017